© Midjourney x What's up Doc
Cet avis favorable a été accordé mardi au Voranigo en tant que premier traitement ciblé du gliome de grade 2 avec mutation d'un gène IDH, après une intervention chirurgicale, précise Servier dans un communiqué.
"Voranigo est la première avancée dans ce domaine spécifique depuis près de 25 ans", souligne le groupe engagé dans les cancers difficiles à traiter.
Diminution du taux de croissance tumorale
L'autorisation de Voranigo aux Etats-Unis s'appuie sur les résultats d'une étude clinique de phase 3 qui a démontré que cette thérapie ciblée prolongeait de manière significative la survie sans progression et le délai avant la prochaine intervention, par rapport au placebo.
D'autres données de cette étude font état d'une diminution du taux de la croissance tumorale et d'une qualité de vie préservée, d'une fonction neurocognitive stable et un contrôle des crises convulsives des patients traités.
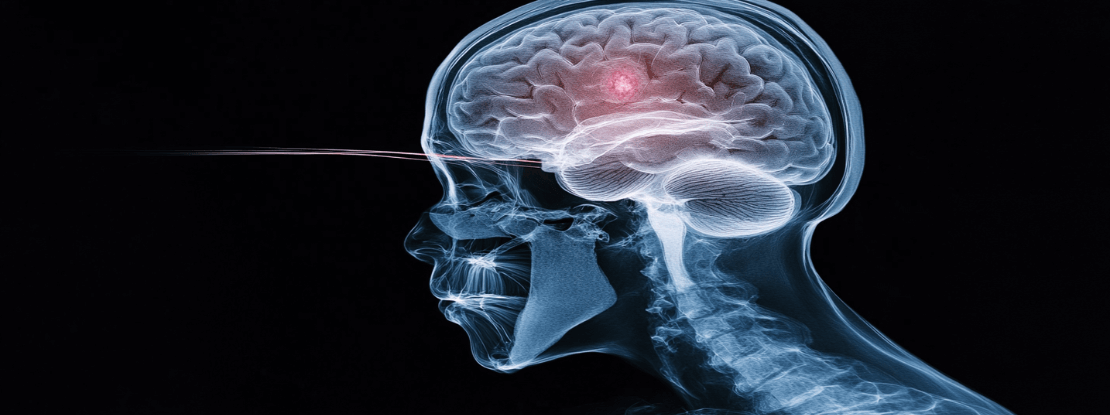
Le médicament, administré oralement et quotidiennement, repose sur une molécule bloquant l'activité d'une enzyme à l'origine de la progression de certains cancers du cerveau, difficiles à traiter.
Les gliomes diffus présentant une mutation d'un gène IDH représentent les tumeurs cérébrales primaires malignes les plus fréquemment diagnostiquées chez les adultes de moins de 50 ans.
Avec AFP
A voir aussi

 Thérapies géniques : en grande difficulté, le seul site industriel français cherche un repreneur
Thérapies géniques : en grande difficulté, le seul site industriel français cherche un repreneur

 Épilepsie : tension sur Alepsal de Teofarma, des alternatives sans caféine existent
Épilepsie : tension sur Alepsal de Teofarma, des alternatives sans caféine existent

 La Commission européenne autorise Rezurock (Sanofi) contre la maladie chronique du greffon contre l’hôte
La Commission européenne autorise Rezurock (Sanofi) contre la maladie chronique du greffon contre l’hôte
 Il délivrait presque autant de fentanyl que de paracétamol : un généraliste girondin devant le tribunal
Il délivrait presque autant de fentanyl que de paracétamol : un généraliste girondin devant le tribunal

 Après une acquisition en oncologie, Novartis s'offre des anti-allergiques nouvelle génération
Après une acquisition en oncologie, Novartis s'offre des anti-allergiques nouvelle génération

 À cause des prix, la France redoute de passer à côté de certains nouveaux médicaments
À cause des prix, la France redoute de passer à côté de certains nouveaux médicaments

 Le Dupixent de Sanofi élargit encore son champ d’action au Japon avec la pemphigoïde bulleuse
Le Dupixent de Sanofi élargit encore son champ d’action au Japon avec la pemphigoïde bulleuse






