© iStock
Modéliser le poumon humain reste un défi majeur. Sa structure en arbre, avec une vingtaine de divisions successives jusqu’aux alvéoles, ses propriétés mécaniques spécifiques liées aux mouvements respiratoires et, surtout, son exposition constante à l’air en font un organe à part. Pendant longtemps, les modèles animaux, notamment les rongeurs, ont servi de référence en recherche préclinique.
Mais ils présentent des différences importantes avec le poumon humain, notamment au niveau des voies respiratoires les plus petites, qui correspondent aux dix dernières divisions de l’arbre bronchique. Or ces zones sont justement atteintes très tôt dans certaines maladies comme la bronchopneumopathie chronique obstructive (BPCO). Cette maladie, principalement causée par le tabagisme, se caractérise par une obstruction progressive et permanente des bronches. Elle touche plus de trois millions de Français, et à ce jour, il n’existe pas de traitement pharmacologique pour guérir ces patients.
Dans le domaine de la santé respiratoire, les organoïdes ont apporté une alternative prometteuse. Ces modèles ont déjà fait leurs preuves. Dans la mucoviscidose, par exemple, des organoïdes dérivés de patients permettent de reproduire les défauts de sécrétion de fluides et de prédire l’efficacité de nouveaux traitements, une avancée majeure vers une médecine personnalisée.
Mais la promesse n’est pas totalement tenue : l’auto-organisation a ses limites. Les organoïdes bronchiques classiques ont une forme de sphères creuses, remplies d’eau et de mucus. Une géométrie bien éloignée de celle des bronches humaines, qui sont des tubes ramifiés. Plus problématique encore : leur architecture fermée rend difficile l’accès à leur intérieur. Stimuler ces modèles par des virus respiratoires, ou bien tester des médicaments inhalés, au cœur des traitements respiratoires, devient alors un défi technique.
Quand les cellules souches prennent forme
Plutôt que de s’en remettre uniquement aux capacités d’auto-organisation des cellules souches, nous avons décidé de guider leur organisation grâce à la bio-ingénierie. Notre pari : imposer une structure tubulaire aux cellules souches pour contraindre leur organisation spatiale, tout en préservant leur capacité à se différencier.
Concrètement, nous avons fabriqué, avec l’aide de nos collègues en biophysique, un moule tubulaire en hydrogel de très petite dimension (environ 0,5 millimètre de diamètre), dans lequel nous avons introduit les cellules souches, purifiées à partir de tissus pulmonaires humains.
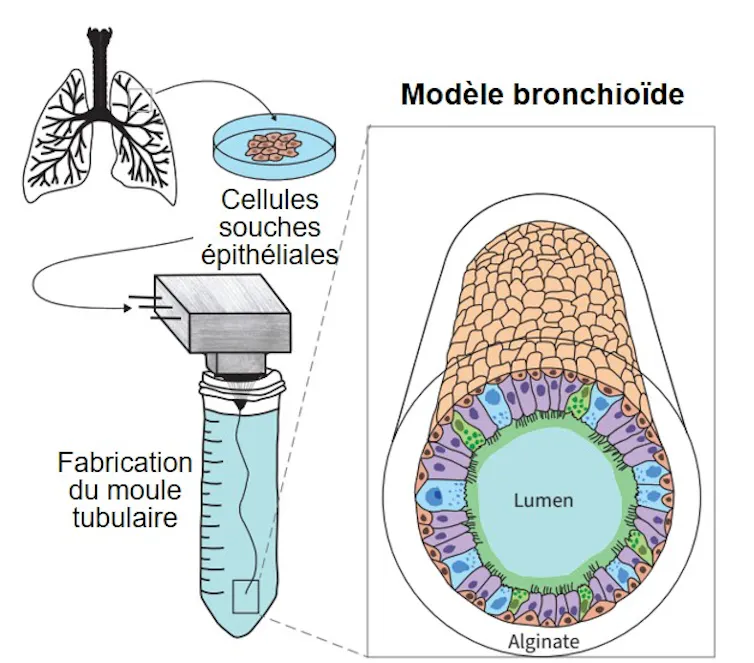
Schéma de la fabrication d’un bronchioïde. Fourni par l'auteur
Les cellules ne se contentent pas de survivre dans cette structure : elles recréent progressivement un épithélium respiratoire fonctionnel, en présence d’un milieu de culture riche en facteurs de croissance. En quelques semaines apparaissent les cellules fonctionnelles de la bronche, les cellules ciliées et des cellules sécrétrices de mucus, le long de la paroi interne du tube. Les cils des cellules ciliées battent bien à la fréquence attendue, soit 15 battements par seconde ! Ces battements sont essentiels pour mettre en mouvement le mucus et assurer la défense de nos bronches face aux agressions de l’environnement.
Surtout, cette architecture ouverte change tout. Pour la première fois, il devient possible de perfuser ces structures et d’y faire circuler de l’air. Il est également possible de les infecter avec des virus respiratoires et d’observer la dynamique de l’infection.
Modéliser la maladie
L’intérêt de notre modèle, que nous avons appelé « bronchioïde », se révèle également lorsqu’on utilise des cellules issues de patients. En recréant des bronchioïdes à partir de cellules de patients atteints de BPCO, nous observons des altérations caractéristiques de la maladie : des battements ciliaires perturbés et une apparition excessive et précoce des cellules sécrétrices de mucus. Autrement dit, le modèle ne reproduit pas seulement des bronches saines, il peut aussi simuler des anomalies pathologiques.
Cette capacité ouvre des perspectives concrètes : mieux comprendre les mécanismes précoces des maladies respiratoires, telles que l’asthme ou la BPCO, tester des traitements dans des conditions plus réalistes et, à terme, adapter les thérapies à chaque patient.
Faut-il parler de « mini-bronches » en laboratoire ? On en est encore loin. Ces modèles restent incomplets. Ils ne contiennent pas, à ce stade, toute la diversité cellulaire du poumon, notamment les cellules de soutien, essentielles au fonctionnement de l’organe. Ils ne reproduisent pas non plus la complexité de l’arbre bronchique, avec son intégration dans les systèmes vasculaire, immunitaire et nerveux. Enfin, les aspects mécaniques dynamiques de la respiration sont généralement absents des modèles organoïdes.
Mais la combinaison de l’auto-organisation et des contraintes physiques imposées par la bio-ingénierie est prometteuse. Les possibilités offertes par cette discipline sont quasiment infinies.
Une équipe grenobloise a récemment réussi à intégrer des organoïdes dans des dispositifs microfluidiques, qui sont des supports contenant des canaux très fins. Ceci a permis de vasculariser les organoïdes, une avancée majeure pour apporter suffisamment d’oxygène et de nutriments à ces structures tridimensionnelles. Une équipe suisse a, quant à elle, reproduit un réseau d’alvéoles grâce à une membrane biologique souple et étirable, qui imite les mouvements de respiration.
Avec l’espoir un peu fou de pouvoir développer grâce à ces outils une médecine plus prédictive et mieux adaptée aux patients !![]()
Isabelle Dupin, Professeure des universités, Université de Bordeaux. Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
A voir aussi

 Diagnostic préimplantatoire et anomalies chromosomiques : les enjeux scientifiques et éthiques du DPI‑A
Diagnostic préimplantatoire et anomalies chromosomiques : les enjeux scientifiques et éthiques du DPI‑A